A genom irányított javítása CRISPR
A genetikai módosítás régen hosszú, drága és kiszámíthatatlan folyamat volt, mert a zigóta sejtmagjába injektált, vagy vírusokkal bevitt DNS darabok véletlenszerűen épültek be a genomba. A legjobb esetben szépen működött, amit terveztünk, mellékhatások nélkül. Leggyakrabban nem kaptunk génkifejeződést. De igen sokszor az is előfordult, hogy a génkifejeződés megtörtént, de a bevitt konstrukció a véletlen beépülés miatt, egy másik génbe szúródott be, ezzel megváltoztatva szabályozását, vagy tönkretéve a gén strukturális részét. Ezzel a transzgénikus állatnak egyéb tulajdonságai is megváltoztak. Nem árt, ha az ember tisztában van ezzel a lehetőséggel, amikor transzgénikus állatot használ. Csak olyat érdemes, ami alaposan tesztelve volt (az persze egy filozófiai kérdés, lehet-e minden, akár ismeretlen változásra is tesztelni).
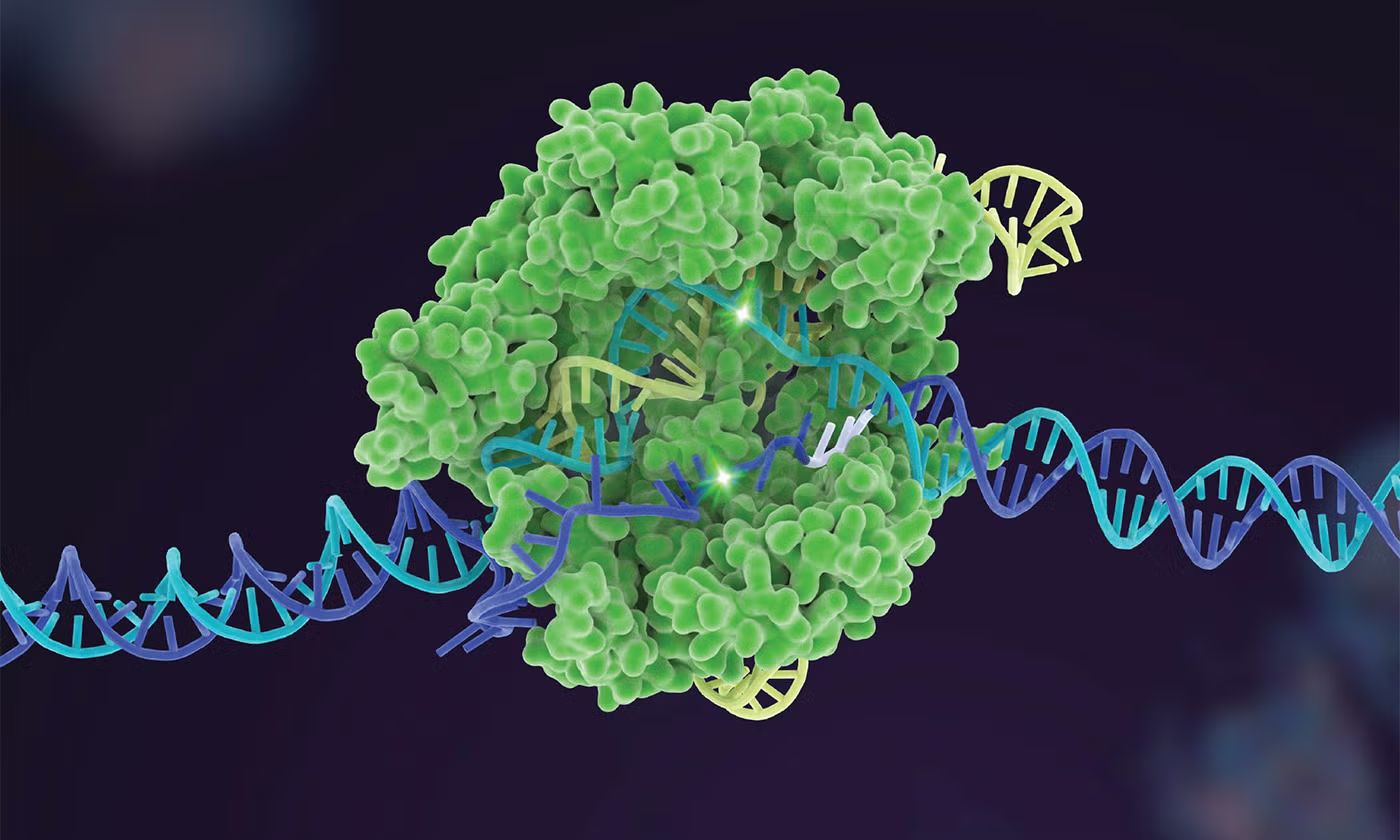 A CRISPR-technológia olyan pontos DNS-szerkesztő ollót adott a kutatók kezébe, amellyel célzottan, mellékhatások nélkül: géneket lehet kiütni, mutációkat lehet javítani vagy beépíteni, élő sejtekben, sőt állatokban lehet megváltoztatni egyetlen betűt a genom szövegében.
A CRISPR-technológia olyan pontos DNS-szerkesztő ollót adott a kutatók kezébe, amellyel célzottan, mellékhatások nélkül: géneket lehet kiütni, mutációkat lehet javítani vagy beépíteni, élő sejtekben, sőt állatokban lehet megváltoztatni egyetlen betűt a genom szövegében.
Segítségével emberi genetikai betegségek hátterében álló pontmutációk állatmodelljei rutinszerűen elkészíthetőek, és meggyógyíthatunk vele mutációkból adódó betegségeket.
Mi is az a CRISPR?
A CRISPR egy baktériumokból származó ún. adaptív immunrendszer. A lényege, hogy a baktériumok elmentik a vírusok DNS-darabjait a genomjukban. Ha ugyanaz a vírus újra támad, egy vezető RNS (guide RNA, gRNA) segítségével a Cas9 nevű fehérje felismeri és elvágja annak DNS-ét. Ez egyfajta bakteriális körözés, a WANTED plakátok alapján kapják el a bűnözőket.
A kutatók ezt a mechanizmust „átprogramozták”: a gRNA-t úgy tervezik meg, hogy a Cas9 ott vágjon, ahol mi szeretnénk a genomot módosítani. Jól tervezett gRNA-val nagyon pontosan, akár egyetlen bázispár is célozható, javítható, cserélhető.
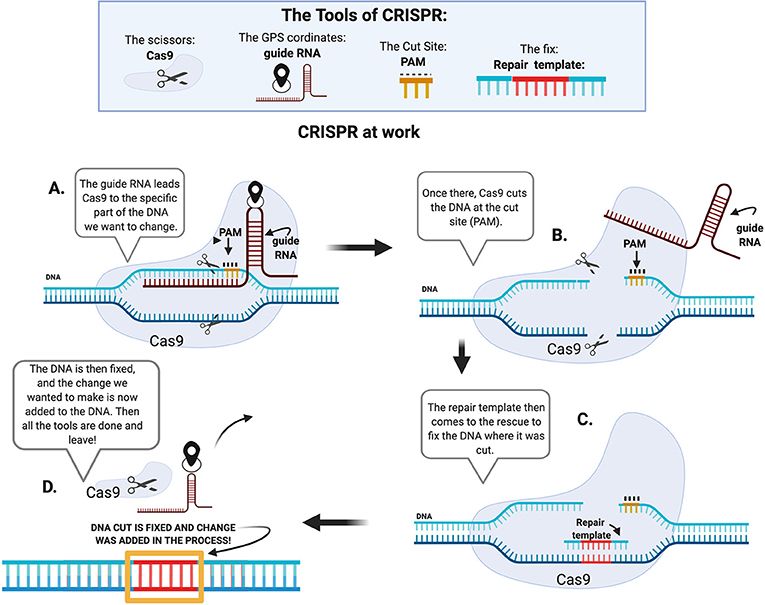
Hogyan történik a CRISPR-szerkesztés?
A kutató kiválasztja azt a DNS-szakaszt, amelyet módosítani akar: pl. egy pontmutációt, amely emberi betegséget okoz (Huntington, SMA, epilepszia, autizmushoz köthető génhibák, stb.). Ennek alapján megtervezi a gNRS szekvenciáját, mely a DNS-en belül a kiválasztott helyre vezeti a Cas9 enzimet. A sejtbe többféleképpen juttathatók be a rendszer elemei: vírusvektorral (AAV), lipid-nanorészecskével (mint az mRNS vakcinák), elektroporációval (pl. zigótákba). A gRNS lényegében egy GPS ami egy adott koordinát keres a genomban. A Cas9 egy „molekuláris olló”, mely a DNS-t a megfelelő helyen elvágja, ez egy célzott kettős szálú DNS törést hoz létre. A vágás után a sejt kijavítja a törést – itt történik a szerkesztés. Két út lehetséges:
a) A sejt gyorsan, de pontatlanul ragasztja vissza a DNS-t -> kis törlések/beszúrások (insertion). Hibás kijavítás -> génkiütés. Ez kikapcsolja (knock-out) az adott gént.
b) Pontos javítás -> génjavítás / mutáció beépítés. Ehhez egy javítósablont is kell adnunk (donor DNS-t), a javításhoz a sejt ezt használja fel, és pontosan azt a mutációt építi be, amit kérünk: -> új pontmutáció bevitele pl. betegségek állatmodelljeinek előállítására), -> hibás gén javítása (gyógyítás).
Miért forradalmi ez idegtudományban?
1. Pontmutációs állatmodellek készíthetők évek helyett, hetek alatt. Régen generációk kellettek egy transzgénikus állathoz. CRISPR-rel egyetlen egér zigótát megvágunk, beépítjük a kívánt mutációt, a született állat már hordozza a génhibát.
Ma rutinszerűen készülnek: autizmushoz kötött SHANK3 mutációk, epilepsziás SCN1A/SCN2A variánsok, neurodegeneratív modellek (pl. ALS, Huntington), dopaminrendszer vagy ioncsatornák célzott módosításai
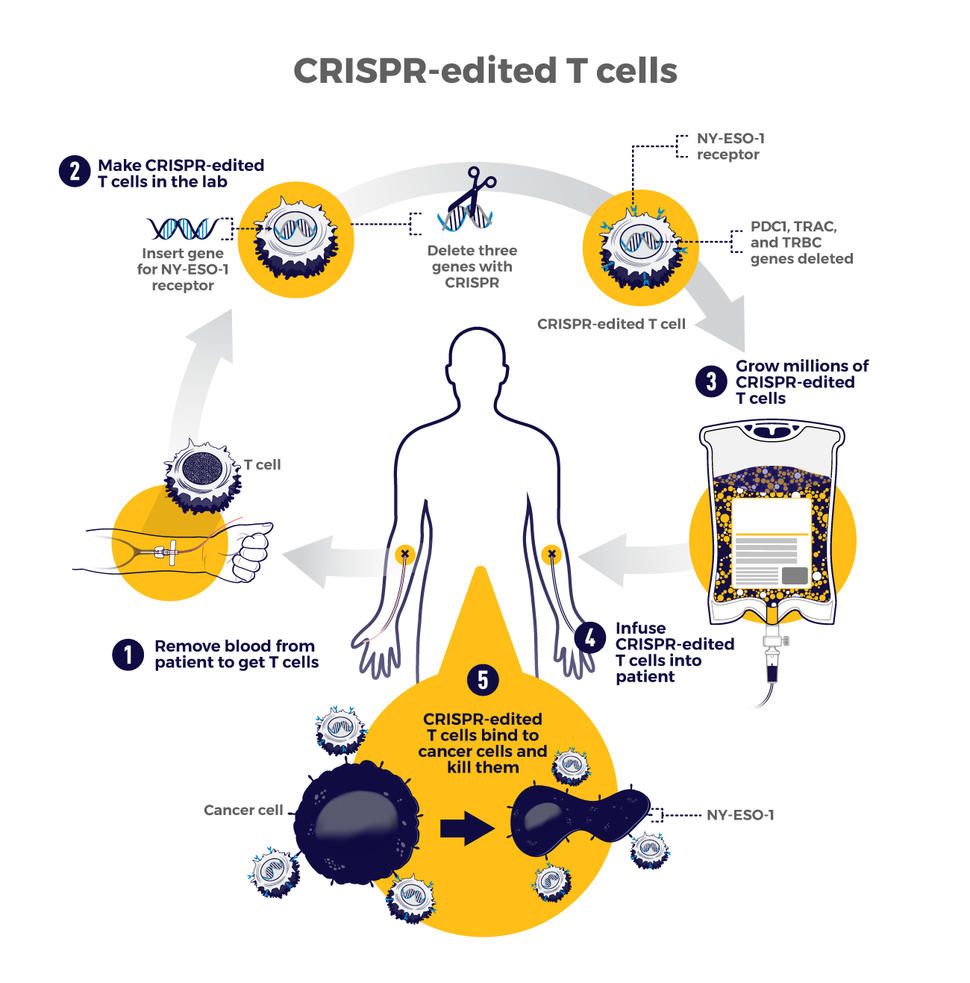
2. Génterápiák. CRISPR egyre gyakrabban kerül a klinikumba, ahol hibás, betegséget okozó géneket javítanak: sarlósejtes vérszegénység, béta-thalassemia, retina betegségek, májenzim-defektusok, izomdisztrófiák, leukémiában T-sejtek módosítása. Az első CRISPR-alapú génterápia 2023-ban kapott engedélyt sarlósejtes vérszegénység gyógyítására, a hibás hemoglobin gént cserélik jóra.
A központi idegrendszerben AAV-vektoros CRISPR-tesztelések zajlanak gerincvelői izomsorvadás, amiotrófiás laterálszklerózis és neuronális ioncsatorna-betegségek kezelésére.
Röviden: A CRISPR úgy működik, mint egy szövegszerkesztő a genomban: a gRNA a kurzor, a Cas9 az olló. A sejt javító rendszere a „helyesírás-ellenőrző”. A kutató dönt arról, hogy törlünk, átírunk vagy beszúrunk egy betűt.
Szerző: Gulyás Attila





